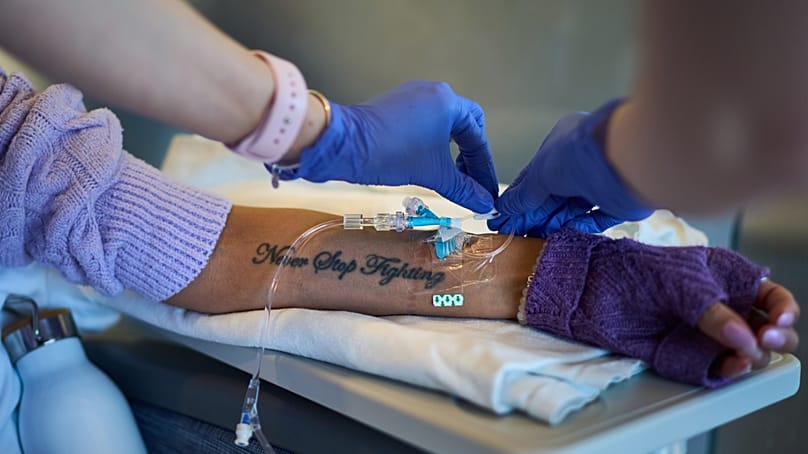
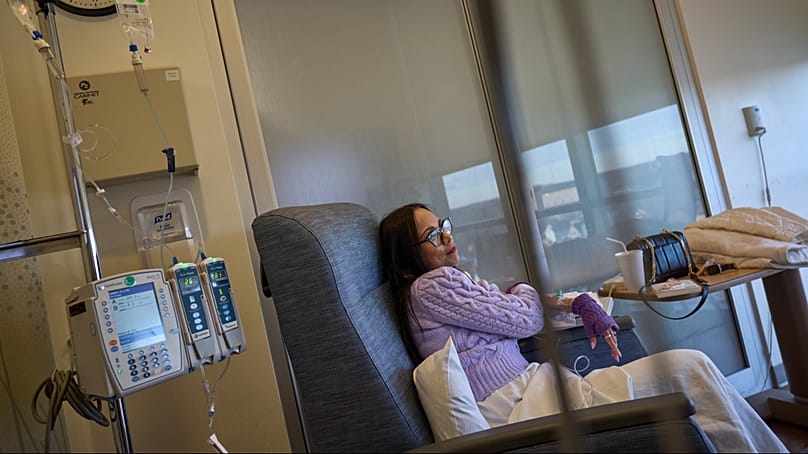
لوپوس، که درمانش دشوار است و شیوعش رو به افزایش است، بخشی از گروه بیماریهای خودایمنی است که میلیونها نفر را در سراسر جهان تحت تأثیر قرار میدهد.
پزشک پشت پزشک به مدت شش سال کهیرها، تورمها، تبها و درد شدید روت ویلسون را نادرست تشخیص دادند یا دستکم گرفتند. او با التماس برای انجام یک آزمایش دیگر در بخش اورژانسی که برای بار دیگر قصد داشت او را بدون پاسخ به خانه بفرستد، جان خود را نجات داد.
 آگهی
آگهی
 آگهی
آگهی
آن آزمایشِ آخر نشان داد کلیههای این زن آمریکایی در حال از کار افتادن بودند. مقصر چه بود؟ دستگاه ایمنیاش در تمام آن مدت به بدن خودش حمله میکرد و کسی متوجه نشده بود.
او گفت: «فقط آرزو میکنم راه بهتری وجود داشت تا بیماران بتوانند به آن تشخیص برسند، بدون اینکه مجبور شوند همه دردها و این، مثلا، بیاعتناییها و گمراهسازیها را تحمل کنند.»
ویلسون مبتلا به لوپوس است؛ بیماری ملقب به «بیماری هزار چهره» بهدلیل تنوع علائمش، و مسیر او تصویری از روی تاریک دستگاه ایمنی ارائه میکند.
لوپوس یکی از مجموعهای از بیماریهای خودایمنی است که تا ۵۰ میلیون آمریکایی و میلیونها نفر دیگر در سراسر جهان را درگیر میکند؛ درمانشان دشوار است، رو به افزایشاند و از بزرگترین معماهای پزشکی محسوب میشوند.
اکنون پژوهشگران با تکیه بر دستاوردهای تحقیقاتیِ سرطان و همهگیری کووید-۱۹ در حال رمزگشایی از زیستشناسیِ پشت این بیماریهای ناتوانکنندهاند. آنها مسیرهایی را آشکار میکنند که به انواع مختلف بیماریهای خودایمنی میانجامد و پیوندهایی میان بیماریهایی که ظاهراً به هم بیربطاند؛ به امیدِ هدف گرفتن علّتها، نه فقط علائم.
این مأموریتی دشوار است. آن «آتش خودی» در اماس اعصاب را میفرساید، در آرتریت روماتوئید مفاصل را ملتهب میکند، در بیماری شوگرن چشم و دهان را خشک میکند، در دیابت نوع ۱ تولید انسولین را از بین میبرد، در میوزیت و میاستنی گراویس عضلات را تضعیف میکند و در لوپوس میتواند سراسر بدن را به آشوب بکشد.
فهرست ادامه دارد: شمار تازه مؤسسه ملی سلامت آمریکا (NIH) ۱۴۰ اختلال خودایمنی را برشمرده است؛ بسیاری نادر، اما در مجموع از علل اصلی بیماریهای مزمن که اغلب نامرئیاند.
«ظاهر شما طبیعی به نظر میرسد. مردم شما را میبینند و فکر نمیکنند چنین بیماری وحشتناکی دارید»، ویلسون ۴۳ ساله گفت؛ کسی که در کنار مدیریت بیماریاش، داوطلبانه به آگاهسازی عموم و حتی پزشکان درباره زندگی با لوپوس کمک میکند.
هرچند هنوز چیزهای بسیار زیادی برای آموختن باقی مانده است، گامهای اخیر برخی متخصصان را به این فکر واداشته که شاید راههای درمان یا پیشگیری دستکم از بعضی از این بیماریها نزدیکتر شده باشد.
در دهها کارآزمایی بالینی، دانشمندان از بخشی از سلولهای ایمنیِ خودِ بیماران بهره میگیرند تا سلولهای سرکشِ تغذیهکنندهِ لوپوس و فهرست روبهگسترِ دیگر بیماریها را از میان بردارند. این روش «درمان CAR‑T» نام دارد و نتایج اولیه این «داروهای زنده» امیدبخش است.
به گفته پژوهشگران، نخستین بیمارِ مبتلا به لوپوس در آلمان در مارس ۲۰۲۱ تحت درمان قرار گرفت و ماه گذشته همچنان در بهبودیِ بدون دارو به سر میبرد.
و دارویی به نام تپلیزوماب میتواند آغازِ علائم دیابت نوع ۱ را در افرادی که سرانجام بیمار خواهند شد به تأخیر بیندازد و پیش از نیاز به انسولین اندکی زمان بخرد. با استناد به آن «شواهد وسوسهکننده»، برنامه پنجساله جدید NIH برای پژوهش در خودایمنی که اگر بودجه بگیرد، توصیه میکند پنجرههای مشابهی برای مداخله در دیگر بیماریهای نهفته دنبال شود.
«احتمالاً هیجانانگیزترین دورانی است که تا به حال در حوزه خودایمنی داشتهایم»، دکتر آمیت سکسانا، روماتولوژیست در مرکز درمانی NYU لانگون در نیویورک گفت.
حمله از داخل
سامانه ایمنی شما راههای متعدد و همپوشان برای شناسایی و حمله به باکتریها، ویروسها و دیگر عوامل مضر دارد. از جمله آموزش دادن سربازان کلیدی – سلولهای T و سلولهای B تولیدکننده پادتن – برای تشخیص بین عوامل بیگانه و آنچه «خودِ شما»ست.
این توازنْ ظریف است، بهویژه با توجه به اینکه گاه میکروبها ویژگیهایی مشابه مولکولهای انسانی میپذیرند تا مدافعان ایمنی را سردرگم کنند و از چنگشان بگریزند. و هرچند دستگاه ایمنی سازوکارهای درونی برای مهار سلولهای ناهنجار دارد، بیماریهای خودایمنی زمانی رخ میدهند که این سامانه از تعادل خارج شود.
شمار زیادی از ژنهای دخیل در کارکردهای گوناگون ایمنی میتوانند افراد را نسبت به بیماریهای خودایمنی شایع مستعد کنند؛ یعنی اگر یکی از اعضای خانواده بیمار باشد، دیگران ممکن است در معرض خطر بیشتری قرار گیرند.
این ژنها میتوانند شامل گونههایی باشند که زمانی نیاکان ما را از تهدیدهای دیرینه، از جمله «مرگ سیاه»، محافظت میکردند اما امروز به دستگاه ایمنی بیشفعال میانجامند.
اما «ژنها همه چیز نیستند»، دکتر ماریانا کاپلان از مؤسسه ملی آرتریت و بیماریهای عضلانیاسکلتی و پوستیِ NIH گفت.
مطالعات نشان میدهد اگر یکی از دوقلوهای همسان دچار بیماری خودایمنی شود، الزاماً دیگری بیمار نمیشود. عوامل غیرژنتیکیِ برانگیزاننده پاسخ ایمنی نقش پررنگی دارند؛ از جمله عفونتها، برخی داروها، سیگار و آلایندهها. در لوپوس حتی یک آفتابسوختگی شدید هم مظنون است.
«در نقطهای یک ضربه دوم یا سوم وارد میشود و دستگاه ایمنی میگوید: دیگر بس است، از پسِ این آسیبها برنمیآیم»، کاپلان که مدیر پژوهشِ خودایمنیِ سیستمیک است، گفت.
زنان بیش از مردان در معرض ابتلا به بیماریهای خودایمنیاند؛ شاید بهدلیل استروژن یا کروموزوم X اضافی. این امر در لوپوس بهویژه چشمگیر است؛ زنان ۹۰ درصد موارد را تشکیل میدهند، اغلب جوانانی مانند ویلسون.
غش کردن و کهیرهای سراسری از دهه سوم زندگیاش آغاز شد و با دو بارداری شدت گرفت. با دو خردسال همراه، نزد پزشکان مختلفی برای تب، تورم، درد مفاصل و کمر رفت تا آن مراجعه سرنوشتساز به اورژانس؛ جایی که خودش درخواست آزمایش ادرار کرد.
ماهها درمانِ طاقتفرسا کلیههایش را نجات داد. اما بیش از یک دهه بعد، ویلسون همچنان با درد روزانهِ ناشی از لوپوس زندگی میکند. خستگیِ عمیق و مهذهنی – مشکل در تمرکز، یادآوری کوتاهمدت و انجام همزمان کارها – کم و زیاد میشود.
درمانها در سالهای اخیر بهبود یافتهاند؛ از استروئیدهای پُردوز و داروهایی که بهطور گسترده دستگاه ایمنی را سرکوب میکنند تا گزینههای تازهای که بر مولکولهای خاص تمرکز دارند. ویلسون ماهانه درمان وریدیِ هدفمند برای لوپوس دریافت میکند و روزانه حدود شش دارو میخورد تا دستگاه ایمنیِ بیشفعال و علائم مرتبط را آرام کند.
بدتر از همه آن چیزی است که «عود» نامیده میشود؛ زمانی که علائم ناگهان و بهطور چشمگیر بدتر میشود. برای ویلسون، به معنای تبهای بالای ناگهانی، پاهایی آنقدر متورم که راه رفتن ناممکن میشود، و دردی شدیدتر است که از چند روز تا یک هفته ادامه دارد. این وضعیت بر کارش در آزمایشگاه پزشکی و وقتش با همسر، پسر نوجوان و دختر دانشجویش اثر میگذارد.
او برای گذر از این روزها به خود میگوید: «زندگی بدی نیست، فقط روز بدی است.»
کاپلان، دانشمندِ NIH، برای این فرسودگی روزمره توضیحی زیستی دارد: همان پروتئینهای التهابی که هنگام سرماخوردگی یا آنفلوآنزا باعث درد و خستگی میشوند، بهطور مداوم در بدنِ مبتلایان به بیماریهای خودایمنیِ سیستمیک مانند لوپوس جریان دارند.
جستوجوی ریشههای علّت
«اینها بچههای من هستند»، دکتر جاستین کوانگ، پژوهشگر همکار در آزمایشگاهِ کاپلان در NIH، گفت؛ در حالی که با دقت سلولها را در انکوباتور بررسی میکرد.
کوانگ کاری بهغایت دشوار انجام میدهد که در بسیاری از آزمایشگاهها انجام نمیشود: او دستههایی از نوتروفیلها، رایجترین سلولهای سفیدِ خونِ بدن، را پرورش میدهد.
این سلولها نخستین پاسخدهندگاناند که به سرعت به محلِ آسیب یا عفونت میرسند، و کاپلان گمان دارد آنها از نخستین سلولهای ایمنیاند که از کنترل خارج میشوند و برخی بیماریهای خودایمنی را برمیانگیزند.
چگونه؟ برخی انواع نوتروفیلها محتویات خود را بیرون میپاشند تا ساختارهایی چسبناک و شبیهِ تار عنکبوت بسازند که میکروبها را به دام میاندازد و میکُشد. نوتروفیلها در این فرایند میمیرند.
اما به گفته کاپلان، بیماران مبتلا به لوپوس و برخی بیماریهای دیگر نوتروفیلهای غیرطبیعی دارند که تارهای بیش از حدی میسازند. تیم او در حال بررسی است که آیا سایر دفاعهای ایمنی این بقایای حاصل را بهاشتباه بیگانه تلقی میکنند و زنجیرهای از واکنشها را برمیانگیزند یا نه.
کاپلان گفت: «فکر میکنیم این یک فرایندِ بنیادیِ آغازین است.»
«میکوشیم بفهمیم چرا رخ میدهد، چرا در زنان بیشتر رخ میدهد، و آیا میتوانیم راهبردهایی بیابیم که جلوی آن را بگیرد بدون اینکه به شیوه دفاع ما در برابر عفونتها آسیب بزند.»
ویژگیِ مشترکِ دیگری هم هست: بیمارانِ مبتلا به شماری از بیماریهای خودایمنی، بهویژه زنان، اغلب در سنین غیرعادی پایین دچار حمله قلبی و سکته مغزی میشوند.
پژوهشِ کاپلان نشان میدهد این ساختارها که بهدرستی «NETS» یا «تلههای خارجسلولیِ نوتروفیل» نامیده شدهاند، ممکن است کلیدِ ماجرا باشند؛ با آسیب به رگهای خونی و تسریعِ تصلّبِ شرایینی که معمولاً در سالمندان دیده میشود.
اما نوتروفیلها بیرون از بدن عمر چندانی ندارند و آزمایش نوتروفیلهای بالغِ خونِ بیمارانِ لوپوسی نشان نمیدهد چگونه از مسیر خارج شدهاند؛ چیزی که نوتروفیلهای «نوزادِ» کوانگ ممکن است به روشن شدنش کمک کند.
بازشناسی تفاوتهای بیماران
هرچه محرکِ آن باشد، لوپوس علائمی بهغایت متنوع و گیجکننده دارد و درمانهایی که میتوانند برخی بیماران را بدون علامت نگه دارند اما برای برخی دیگر کارساز نیستند. این نشان میدهد «لوپوس یک بیماریِ واحد نیست»، کاپلان گفت. «آنچه لوپوس مینامیم احتمالاً نمایندهِ شرایطِ گوناگونی است که برخی عوامل مشترک دارند».
اینکه چگونه لوپوس را زیرگروهبندی کنیم روشن نیست. اما بیماری دیگری، آرتریت روماتوئید (RA)، شاید سرنخهایی ارائه کند. این بیماری که شاید بیش از همه با انگشتانِ دردناک و تغییرشکلیافته شناخته شود، میتواند به هر مفصلی و حتی برخی اعضا حمله کند و گاه به ریهها آسیبِ فیبروتیک بزند.
مانند لوپوس، درمانِ RA مبتنی بر آزمون و خطاست و دانشمندان در حال بررسی عواملِ زمینهای مختلف برای توضیح چراییِ این موضوع هستند. در یک مطالعه، تیمی بینالمللی با استفاده از نمونههای کوچکِ بافتِ مفصلِ بیماران شش زیرگونه التهابیِ RA را بر پایه الگوهای سلولی، نحوه خوشهبندی و فعالیتشان شناسایی کرد.
«این رویکرد طرز فکر ما درباره بیماری را تغییر داد»، هریس پرلمان، رئیس روماتولوژیِ دانشگاه نورثوسترن و یکی از نویسندگانِ همکار، گفت. او افزود اکنون پژوهشگران سلولهای موجود در بافتِ مفصل را پیش و پس از شروع یک داروی جدید مقایسه میکنند تا ببینند آیا میتواند به راهنماییِ انتخابهای درمانی کمک کند یا نه.
زندگی با لوپوس
ویلسون آموخت که در فضای باز ضدآفتاب بزند و کلاهی بزرگ بر سر بگذارد و انرژیاش را جیرهبندی کند تا شاید از عودها جلوگیری کند. وقتی بچههایش بهسن مدرسه رسیدند، او هم به مدرسه برگشت، مدرکهایی گرفت که به کارهای پژوهشگاهی و علم داده منتهی شد و به درک بهترِ بیماری و درمانهای خودش کمک کرد.
یک روز روماتولوژیستِ وقتش از او خواست به چند سؤالِ دانشجویان پزشکی پاسخ بدهد. ویلسون به یاد دارد بسیاری میدانستند «لوپوس در کتاب درسی چگونه به نظر میرسد»، اما از منظرِ بیمار بیخبر بودند.
«فهمیدم، خدای من، باید شروع کنم به حرف زدن درباره این موضوع».
اکنون این چگونه است: یک عصرِ فوریه گذشته، ویلسون با هیجان و اضطراب از دیدارِ سرانجامی با چند عضو از گروهِ حمایتِ آنلاینِ لوپوس خود سرشار بود. در دانشکده پزشکی یومسچان (UMass Chan)، ویلسون دو زن و دو مرد را با آغوشی گرم خوشامد گفت.
آنها علائم و درمانها را به اشتراک گذاشتند و داستانهای پرحسرتی از خویشاوندانِ خیرخواهی گفتند که اصرار داشتند فقط بیشتر بخوابند تا با خستگیِ لوپوس بجنگند؛ خستگیای که استراحت از پسِ آن برنمیآید.
یک ماه بعد، ویلسون راهی واشنگتن شد برای نشستی که توسط «اتحادِ پژوهشِ لوپوس» برگزار شده بود؛ جایی که از دانشمندان و پژوهشگرانِ شرکتهای دارویی خواست به گزارشهای بیماران از تغییرات در زندگی روزمرهشان گوش دهند، از جمله اینکه آیا درمانِ جدید به مهذهنی کمک میکند یا نه.
او گفت مطالعات دارویی که علائم جسمی و نشانگرهای خونی را میسنجند «فقط نیمی از داستان را ثبت میکنند». «اگر درمانی به من اجازه دهد واضح فکر کنم، در زندگیام مشارکت داشته باشم، و همان کسی باشم که میدانم زیرِ همه اینها هستم، آن به همان اندازه کاهشِ التهاب اهمیت دارد».
در حالی که پزشکش هنوز درمانهای آزمایشی را توصیه نمیکند، ویلسون بهتازگی به «مطالعه نقطهعطفِ لوپوس» پیوسته است؛ پژوهشی که نمونههای زیستیِ ۳٬۵۰۰ بیمار را پیگیری میکند تا تفاوتهای بیماری بهتر درک شود. هر بار که عود رخ میدهد، ویلسون انگشتش را برای گرفتن نمونه خون میخراشد و آن را به اشتراک میگذارد.
«برای من مهم است که صدایی برای بیماران هم باشم، چون به خودم فکر میکنم و به آنکه در همان آغاز چقدر تنها بودم»، ویلسون گفت.
«برای مدت طولانی هرگز نمیخواستم دربارهاش حرف بزنم. مخصوصاً درباره بچههایم؛ میخواستم بدانند که حالِ من خوب خواهد شد. پس آرایش میکنی و رژلبت را میزنی و سه رنگِ اصلاحکننده زیر چشم را میگذاری و ادامه میدهی.»